О. А. Омельчук,a,b@1 Л. Н. Лысенкова,a Н. М. Белов,a А. М. Королев,a Л. Г. Деженкова,a Н. Э. Грамматикова,a,c О. Б. Беккер,d В. Н. Даниленко,d А. Е. Щекотихинa,b@2
aИнститут по изысканию новых антибиотиков имени Г.Ф. Гаузе, 119021 Москва, Российская Федерация
bРоссийский химико-технологический университет имени Д.И. Менделеева, 125047 Москва, Российская Федерация
cПервый Московский государственный медицинский университет имени И.М. Сеченова, 119991 Москва, Российская Федерация
dИнститут общей генетики Российской академии наук имени Н.И. Вавилова, 119333 Москва, Российская Федерация
DOI: 10.6060/mhc180795o
Макрогетероциклы 2018 11(3) 322-328
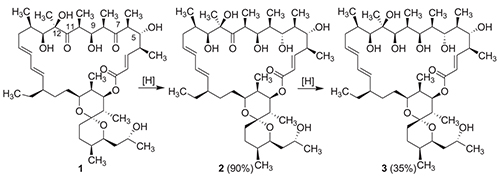
Найдены методы регио- и стереоселективного восстановления карбонильных групп олигомицина А (1). При действии триацетоксиборгидрида натрия в уксусной кислоте на исходный антибиотик 1 образуется (7S)-дигидроолигомицин А (2), дальнейшее восстановление которого боргидридом натрия в этаноле дает (7S,11R)-7,11-тетрагидроолигомицин А (3). Структура полученных производных 2, 3 доказана методами ЯМР-спектроскопии и масс-спектрометрии. Исследованы антимикробные свойства и антипролиферативная активность новых производных в сравнении с исходным антибиотиком. Показано, что восстановление карбонильных групп олигомицина А приводит к снижению активности производных 2, 3 в отношении всех протестированных культур за исключением линии клеток миелоидной лейкемии человека К-562 и ее сублинии с множественной лекарственной устойчивостью К-562/4. Биологическая активность (7S,11R)-7,11-тетрагидроолигомицина А незначительно отличается от активности (7S)-дигидроолигомицина А, что говорит о большем влиянии кето-группы в положении 7, чем в положении 11 на антибиотические свойства.
С полным текстом статьи можно ознакомиться на английской версии сайта
References: